生物药物通过培养,收集,经过层析介质的纯化,最终得到符合要求的生物药物产品。在生物药物的生产过程中,层析技术是其中最关键的步骤。它可以去除包括宿主的蛋白、核酸、脂类,培养过程中的代谢产物、内毒素、杂菌以及可能的层析填料的泄漏,试剂中的杂质。层析介质是一种消耗品,层析介质的经过一段时间使用,清洗后,污染物的残留量超过了安全水平,那么层析介质的寿命就到期了,只有更换新的层析介质才能保证生物药品的质量。基于生产成本的控制,层析介质一般需反复多次使用,但在连续使用过程中,其性能指标会随着使用周期的延长发生变化,至使层析效果下降,从而影响相应产品和中间产物的质量及临床安全性。
1.层析介质在工艺中纯化位置
在三步纯化工艺中,直接捕获(粗纯)→中度纯化→精纯。不同的纯化步骤,其纯化工作的目的不同。以捕获阶段为例,其目的是从细胞培养液中一步捕获目标样品,大幅度提高目标蛋白的纯度。所以此步骤的工作面临的是物料中有大量杂质,同时也需要强烈的清洗条件,因此捕获步骤的层析介质的寿命相对较短。其他步骤的填料,其本身累积的杂质少,所以寿命相对较长。
2.层析介质类型
离子交换、疏水的配基为小分子的配基; 亲和介质的配基一般为特殊的蛋白质。亲和介质的配基一般稳定性稍差,不耐受酸、碱等较强的清洗条件,所以对清洗的条件要求比较严格,较强的试剂清洗可能导致配基的脱落或降解。但是,温和的试剂的清洗效果较差,长期的杂质的积累,也会最终造成层析介质的寿命缩短。
3.层析柱的维护
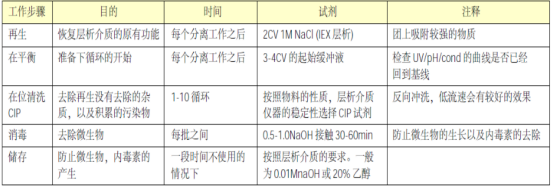
层析介质的维护是层析介质寿命的关键。层析介质的维护包括层析介质的清洗,消毒,储存。(试验中,同样需要测试储存用溶液对细菌和真菌的抑制作用。)选择用于清洁、消毒层析介质和过滤膜包的溶液,需要依据供应商的推荐、供应商的化学相容性数据和(或)制药企业自己的试验结果。另外也要依据溶液去除工艺杂质、使微生物杂质失活和降低内毒素水平的能力。表1 总结了各个步骤的作用:
表1 层析柱的维护程序

4.其他,例如整个层析系统的组成,层析柱的装柱质量等
在生产进程中,一份针对耗材使用周期的确认方案需要遵循一系列预先定义的参数。判断层析介质的寿命主要以下列参数,如果已经超过预期设定标准,则需要更换层析介质了。
1.产品的性质:产品的纯度(SEC、CEX)、收率;
2.杂质的性质:杂质的含量 (HCP、DNA、聚体);
3.层析介质在生产中的参数:载量、洗脱峰的保留时间,洗脱峰的对称性等;
4.层析介质的运行的参数:压力、流速、柱高、再生、在平衡的UV/pH/Cond 等参数;
5.泄漏:层析介质的配基泄漏 (尤其为亲和介质的配基泄漏是否在规定的水平)
缩小模型中的前瞻性使用寿命研究数据能否被法规监管部门接受,很大程度上取决于该缩小模型能否代表商业化生产规模的性能,因此在进行前瞻性使用寿命研究前,需对该缩小模型进行适用性确认和评估。一旦缩小规模实验结果被证明与大规模工艺的结果接近,那么用小规模实验来推测层析介质和可重复使用膜包的寿命就无可非议。用小规模实验的好处是,它可以与生产操作完全独立进行。这些试验结果可以为设定初始的耗材寿命和耗材预期基本性能提供依据。另外,小规模试验可以为‘用过的介质’提供一个理论模型,该模型可以用来评估介质使用一段时间,对病毒的清洁能力。
表2 scale-down model参数

直接捕获阶段的Protein A 在抗体纯化过程中有举足轻重的作用,它可以将目标蛋白的浓度提高到95%以上,然而,唯一的缺点就是价格昂贵。因此,scale down 模型在该填料的寿命研究上将对生产何时更换填料以及验证工作有前瞻性的指导意义。下面是案例分析的简介,其中,表3是BMS公司用缩小模型的研究信息。
表3 案例信息

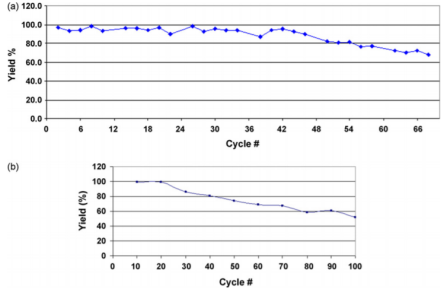
图1 Protein A 寿命研究之回收率 (a)Sepharose FF; (b) MabSelect.
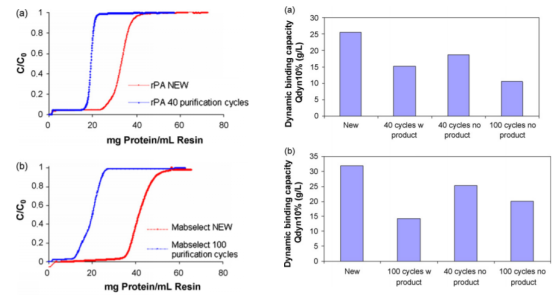
图2 Protein A 寿命研究之DBC (a)Sepharose FF; (b) MabSelect.
随着使用次数的增加,Sepharose FF和MabSelect 回收率都有不同程度的降低(图1),尤其是Sepharose FF,这主要是两者的填料基架不同的原因,MabSelect是高度交联的琼脂糖,较Sepharose FF更稳定。类似的,填料的重复使用也造成DBC的下降(图2),这间接说明填料与蛋白传质性能的部分丧失有关,蛋白结合变少导致回收率的降低。
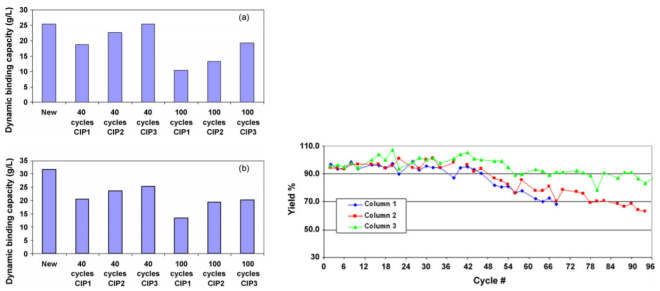
图3 Protein A 寿命研究之CIP对DBC和回收率的影响 (a)Sepharose FF; (b) MabSelect.
CIP1: no strip, regeneration with 3CVs of 0.1N NaOH;
CIP2: strip with 3CVs of 0.1 M phosphoric acid, regeneration with 3CVs of 50 mM NaOH, 0.5 M NaCl;
CIP3: no strip, regeneration with 3CVs of 0.1N NaOH.
图3表明再生对填料DBC和收率的影响,主要的原因是清洁效果的强弱会严重影响配基的脱落,影响蛋白与配基的结合,进而影响回收率。在Fc融合蛋白的寿命研究中,由于最大的操作负载量接近树脂的动态结合能力,因此对步进率的影响可能更为明显。
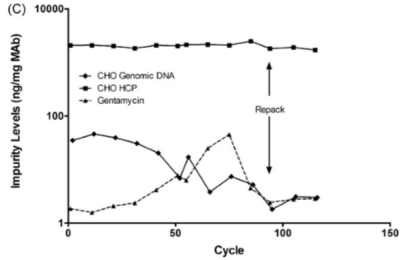
图4 Protein A 寿命研究之杂质去除的研究
有研究表明,MabSelect Sure至少在100cycles回收率能够得到保障,杂质的去除效果如图4所示,对HCP的去除作用没有改变,DNA下降比较明显。
建立层析介质使用寿命的研究方案的合理性和科学性,是该层析介质使用寿命被法规监管部门批准的前提和基础。每种层析介质的使用寿命均应依据专门设计的研究方案进行实验数据的收集和分析,通过缩小模型的前瞻性使用寿命研究方案,获得某一介质使用寿命的实验数据并进行统计学分析,从而确定该层析介质的使用寿命,并在常规商业化生产过程中,对该使用周期进行同步监测和确认。
参考文献
1)SoferG. Biorprocess;establishing resin lifetime,Bioprocess International,2003,1(1): 64-69.
2)O'Leary RM,Feuerhelm D, Peers D, et al. Determining the useful lifetime of chromatography resins [J]. BioPharm, 2001, 14(9): 10-17
3)Jiang C , Liu J , Rubacha M , et al. A mechanistic study of Protein A chromatography resin lifetime[J]. journal of chromatography a, 2009, 1216(31):5849-5855.
4)A. Rathore, G. Sofer, in: A. Rathore, G. Sofer (Eds.), Process Validation in Manufacturing of Biopharmaceuticals, CRC Press Taylor and Francis, Boca Raton, FL, 2005, p. 169.
5)C. Bussineau, R. Seely, G. Lovitt, J. Fernandez, G. Blank, E. Brandreth, D. Conrad, R. Devine, R. Ferris, K. de Heyder, R. Juffras, P. Levy, W. List, M. Munk, B. Neely, S. Notarnicola, R. O’Leary, H. van Deinse, PDA Technical Report #42, 59 (2005) 1.
6)Process Validation of Protein Manufacturing.
识别微信二维码,添加生物制品圈小编,符合条件者即可加入生物制品微信群!
请注明:姓名+研究方向!

本公众号所有转载文章系出于传递更多信息之目的,且明确注明来源和作者,不希望被转载的媒体或个人可与我们联系(cbplib@163.com),我们将立即进行删除处理。所有文章仅代表作者观点,不代表本站立场。