双抗的纯化策略

截至2020年4月16日,全球累计批准上市92款抗体药物(不包括已退市),其中FDA累计批准上市90款。其中,双抗占据了一个非常重要的位置。截至目前,已有20多个不同的商业化技术平台可用于双抗的开发,设计的双抗分子结构60多种, 3个双抗获批上市,超过85个双抗处于临床开发阶段。
双抗的研发历史经历了类似的发展—困境—突破的过程。从上个世纪60年代,科学家们首次尝试从多克隆抗体血清中分离出两个Fab片段,并在体外重新组装成双特异的F(ab‘)2分子开始,经过了20多年的努力,Fab、Fv、scFv、VHH等结构的特异性终于逐步被研究清楚,从而突破了一直阻碍双抗开发的免疫原性、稳定性、溶解性,生物学机理以及工业化生产等困境。
为了让大家更好地了解双抗,特别是了解双抗的下游纯化工艺,佰傲谷整理了近年来双抗的一些有代表性的纯化策略。
双特异性抗体 (bispecifc antibody, BsAb) 是指含有两种特异性抗原结合位点的人工抗体,可以同时与靶细胞和功能细胞进行相互作用,进而增强肿瘤细胞杀伤功能。
双抗主要通过基因重组技术进行生产,有多种多样的分子设计类型,满足双抗分子识别两种不同抗原的能力。根据是否含有 Fc 片段可以将双抗分为:IgG-like 和 Non IgG-like 两大类[2] (图1-1)。

这类抗体的分子含有Fc区,因此保留了ADCC和CDC效应,可以增强肿瘤的杀伤效果,同时使双抗分子具有半衰期长,稳定性好的优势。然而,为了尽可能多的获得我们需要的分子类型,在重组表达这类双抗分子时需要进行一些分子的理性设计。图1-2[3]显示了,如果没有理性设计,在表达某双抗 (4-chain heterodimer) 时,理论上会伴随产生10种以上的副产物,主要包括重链之间错配引起的同源抗体 (homodimer Fc species),轻链与重链之间错配引起的异源抗体(heterodimeric Fc species),结构不完整的片段抗体,如半抗体 (half antibody) 或3/4 抗体,以及轻链聚集体 (light chain dimer),重链聚集体 (heavy chain dimer) 等等。
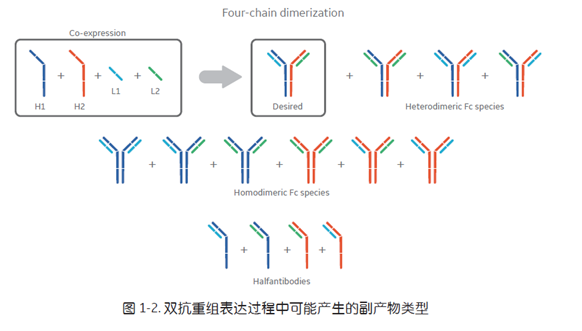
截止目前,科学家们已经找出多种巧妙的分子设计策略,来降低上述副产物的产生。表1-1[4]分别给出了可用于有效降低重链同源错配 (HC homodimerization) 以及轻链与重链错配 (HC-LC misparing) 的分子设计策略。其中,最经典的要属降低重链同源错配的 KiH,即 Knob-into-hole 技术,以及降低轻链重链错配的 CrossMab 技术。

然而,所有分子设计策略都只能尽量降低某类副产物的产生,而不能完全消除全部的副产物。不仅如此,在双抗的重组表达过程,还不可避免的会产生不完整的片段抗体以及聚集体。所有这些都给双抗分子的下游工艺开发提出了挑战。如何快速拉通双抗分子的下游纯化工艺路线,从众多不同层析原理的填料中筛选出合适有效的层析填料,并确定合理的参数范围,成为每个双抗下游纯化工艺开发人员的必答题。
面对这个问题,我们在第二部分给出了切实可行的 IgG-like 类型双抗分子的纯化平台工艺,并且详细介绍了几类主要的副产物,比如 homodimer, half antibody, light chain related impurity, aggregate 等的有效纯化方法。
除了上述介绍的 IgG-like 类型的双特异性抗体外,还有一类双抗分子,即各种不含有 Fc 区的 Non IgG-like 的双特异性抗体。这些双抗分子结构各异 (图1-1) ,在临床应用上因为分子体积小,具有免疫原性低,组织穿透能力强的优势;在表达策略上,由于不需要复杂的翻译后修饰,可以灵活选择大肠杆菌,酵母菌, CHO 细胞等多种表达体系。但是,由于其分子结构中不含有 Fc 区域,在下游纯化工艺选择上,就不能利用成熟的蛋白 A 亲和层析,而须选用其他可行的纯化平台来达到有效纯化的目的,那么,如何根据这些结构千差万别的 Non IgG-like 双抗分子的序列特色,快速选择合适的纯化平台,成为从事这类分子纯化工艺开发人员的迫切需求。同时,如果选择了 CHO 以外的其他表达体系,比如如大肠杆菌,虽然可能在生产周期和经济成本上,相较于CHO体系,取得一定的优势,但是在下游工艺开发中,就必须要考虑内毒素,色素等过程相关杂质如何有效去除的问题。
因此,我们在第三部分详细介绍了适合各类分子结构的 Non IgG-like 双抗的下游纯化平台,列出了不同表达体系在NonIgG-like 双抗表达上的特点,并给出了不同表达体系下,主要过程相关杂质的纯化方法。
最后,充分讨论了产品相关杂质 (如homodimer,halfantibody),过程相关杂质 (如内毒素,色素) 的纯化策略。在第四部分加深了对纯化盲点的解析,讨论了工艺稳健性的问题,提出了工艺稳健性的重要影响因素—填料批间差,并给出了科学的评估方法。
此类双抗通过重链配对形成 IgG 样结构,对于 IgG-like BsAb,我们给出的相应的纯化路线图 (图2-1) 可以去除此类BsAb 中的 homodimer, half antibody, light chain related impurity 和 aggregate 等常见产品相关杂质。针对 heavy chain related impurity 的话,去除方法相对简单,一般也可选择 Capto L, KappaSelect 又或者是 LamdaFabSelect 的亲和填料去捕获,直接流穿重链相关杂质,例如 HH。
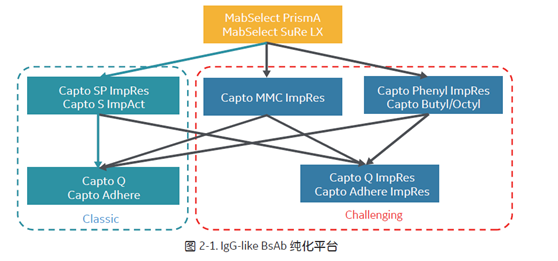
一般而言, homodimer 很难去除,因为其物理化学性质都与目标 BsAb 很相似。Homodimer 的去除可以充分利用BsAb 的分子结构设计特点,通过亲和力差异性与电荷及疏水性差异来进行纯化。
2.1.1 MabSelect PrismA/MabSelect SuRe LX
通过阻断重链恒定区 Protein A 结合位点的分子设计策略可有效简化同源二聚体的去除 (图2-2)。
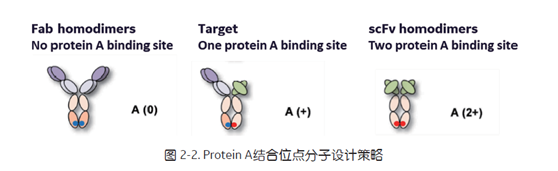
在此类设计中,可简单通过 Protein A 亲和层析有效去除同源二聚体 (图2-3)。经SDS-PAGE分析后,目的 BsAb 纯化可达96%[5]。
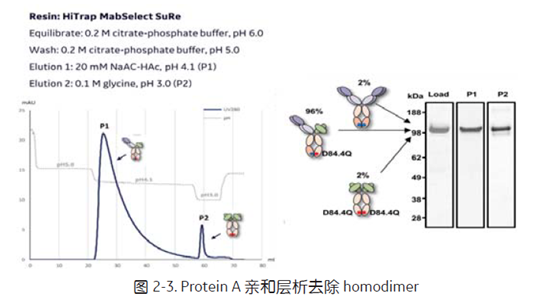
MabSelect PrismA, MabSelect SuRe LX 载量更高,耐碱性更强,尤其是粒径 60 μm的 MabSelect PrismA 可耐受 1.0 M NaOH, 150 cycle 的清洗,且具有更高的分辨率。
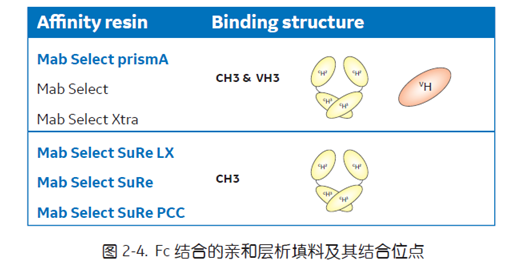
2.1.2 Capto SP ImpRes/Capto Q ImpRes
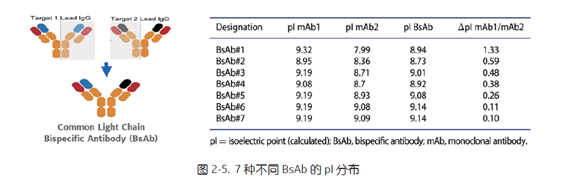
去除 homodimer,可以利用其与目标 BsAb 的电荷差异,pH梯度会比盐梯度表现出更高的分辨率。即使两种亲代抗体之间的 pI 差异非常小 (即 0.1 个 pH 单位),也可以使用高度线性的 pH 梯度分离目标 BsAb 与 homodimer[6]。图2-5 列出了 7 种不同 BsAb 的 pI 分布, BsAb#1 的两个亲代抗体 (homodimer)之间 pI 差距最大,为 1.33,相对应的 BsAb#6 和 BsAb#7 的 homodimer 之间 pI 就很小,仅为 0.1。
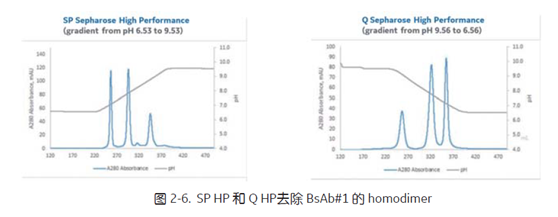
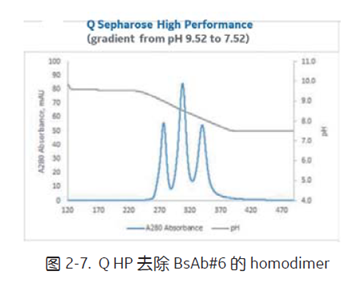
对于BsAb#1 来说,选择高分辨率的 SP Sepharose High Performance 和 Q Sepharose High Performance,通过 pH 梯度洗脱的方式,均可实现 homodimer 与目标 BsAb 的有效分离 (图2-6)。对于 BsAb#6 来说,选择 Q HP 的 pH 梯度洗脱方式,即使 homodimer 与目标 BsAb 之间 pI 只差 0.05 个 pH 单位,也能实现有效分离 (图2-7)
新一代 Capto SP ImpRes 与 Capto Q ImpRes 同样是高分辨率的离子填料,其 Capto 基架具备良好的压力流速性能,为后续工艺的生产放大提供了保障,可作为高分辨率类填料中的优先选择。
2.1.3 Capto MMC ImpRes/Capto Adhere
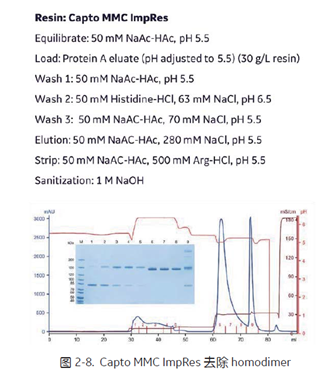
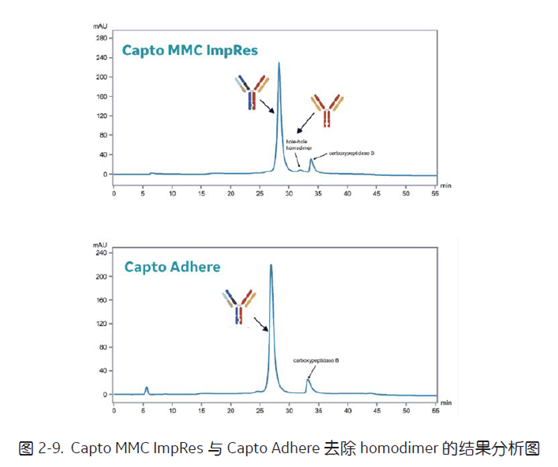
Homodimer 的去除也可以利用其与目标 BsAb 的电荷及疏水性差异,复合模式层析填料 Capto MMC ImpRes, Capto Adhere 同时具备电荷作用与疏水作用,可有效去除 homodimer[7]。案例中 pH 5.5 的上样条件下 (图2-8), homodimer 结合能力略弱于目标 BsAb,因此在 Capto MMC ImpRes 的结合洗脱的过程中加入两步淋洗步骤 Wash 2 (50 mM Histidine-HCl,63 mM NaCl, pH 6.5) 与 Wash 3 (50 mM NaAC-HAc, 70 mM NaCl, pH 5.5),从图2-9 中可明显看出 Capto MMC ImpRes 去除了大量 homodimer,但仍然残留微量的 homodimer,经过进一步的 Capto Adhere 精纯,最终将 homodimer 彻底去除。最近的研究报告中,也有发现在略低于常规 pH (比如 pH 4.5) 时 (一般抗体纯化常使用 pH 5.5), Capto MMC ImpRes 在 holehole homodimer 和 heterodimer 的分离上分辨率提高。另外,还可以通过在淋洗和洗脱 buffer 中添加 5% 的 PEG 3350 来进一步提高分辨率。
Half antibody 是 BsAb 生产中的一种常见杂质,是由无法形成 homodimer 的重链的过表达而导致的。Half antibody与目标 BsAb 差别较大,一般可以通过
亲和力差异性
与
电荷性质差异
来进行纯化。
2.2.1 MabSelect PrismA/MabSelect SuRe LX
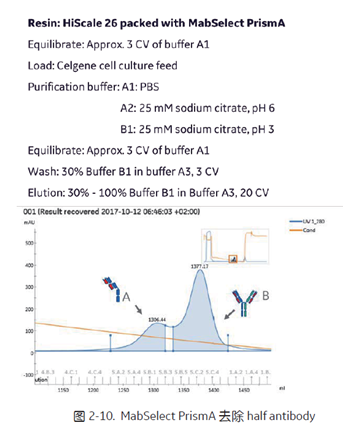
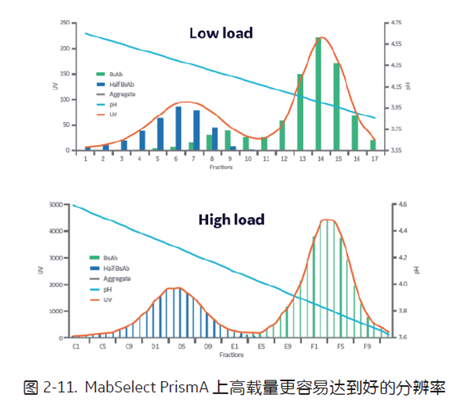
Half antibody 只含有一个 Fc 区域,因此它结合 Protein A 填料的能力比含有两个 Fc 的分子较弱一些。在 protein A亲和层析阶段进行 pH 线性梯度洗脱, half antibody 将会比目标物略早洗脱。图2-10 中, MabSelect PrismA 通过 pH 线性梯度洗脱的方式,将 half antibody 与目标 BsAb 显著分离,同时还可以去除一些其他杂质[8]。一般情况下,经 MabSelect PrismA 这一步后,保持收率在 85% 的前提下,纯度仍然可达 90% 以上。同时研究表明,在 MabSelect PrismA 亲和层析中,上样载量越高, half antibody 与目标 BsAb 分离效果越好,即高载量更容易获得更高的分辨率 (图2-11)
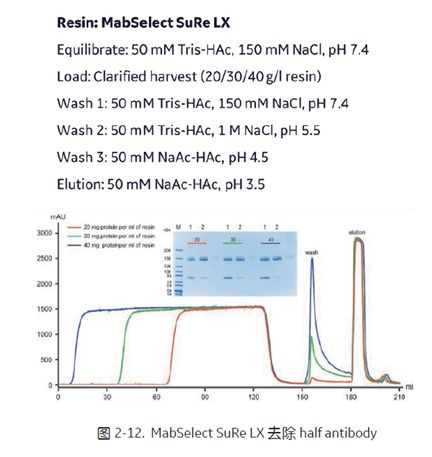
基于 pH 线性梯度的结果,可以进一步将洗脱条件优化为等度 pH 洗脱。中间淋洗条件的优化也是非常关键,中间淋洗pH需要足够低以保证 half antibody 的有效洗脱,同时保证目标 BsAb 结合在填料上。最优的中间淋洗 pH 与上样量有关,中间淋洗 pH 的高低分别对应于上样量的高低,所以需要平衡好 half antibody 的去除率和收率。图2-12 中, 在选择 MabSelect SuRe LX 的前提条件下,优化得到 50 mM NaAc-HAc, pH 4.5 的中间淋洗条件,并且在此淋洗条件下优化上样载量,发现载量越高, half antibody 的去除效果越好,但伴随着收率的降低,案例中,权衡之后,选择 30 g/L resin的上样载量,去除大部分 half antibody 的同时收率达 82.4%[7]。
Capto MMC ImpRes,在合适的实验条件下可以有效去除 half antibody。Capto MMC ImpRes 具有 CEX和疏水填料的特性。如图2-13 所示,pH 线性梯度实验可有效分离 half antibody[8]。Half antibody 的结合力比目标 BsAb 要弱一些,洗脱会比较早。基于这样的结果,后续可以优化一个合适的中间清洗条件,选择性清洗 halfantibody,然后通过 step elution 洗脱目 标BsAb。
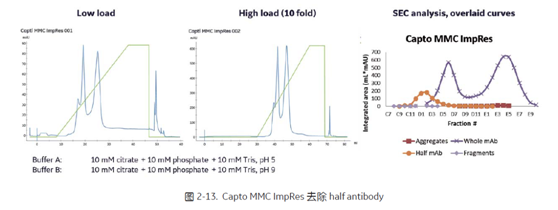
2.2.3 Capto SP ImpRes/Capto S ImpAct
在 half antibody 的 pI 与目标 BsAb 的差异比较显著的情况下,我们也可以通过 CEX 进行纯化。图2-14 和图2-15 分别是 Capto SP ImpRes 和 Capto S ImpAct 通过 pH 线性梯度洗脱的方式分离 half antibody[8], SEC 分析结果,与 CaptoMMC ImpRes 结果相似, Capto SP ImpRes 和 Capto S ImpAct 均可以有效去除half antibody,并且达到比较高的分辨率。
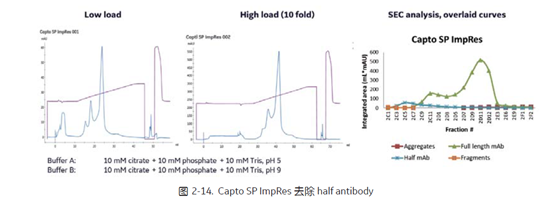
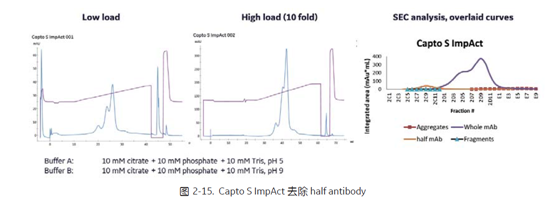
2.3 Light chain related impurity 的去除
Light chain related impurity 主要是 BsAb 生产中的出现的一些分子片段,其中 HHL (完整 BsAb 上缺了一条轻链) 和HHLLL (完整 BsAb 上多了一条轻链) 为最难去除的片段杂质。但是即使是与目标 BsAb 差别很小的 HHL 与 HHLLL,通过电荷或/及疏水性差异也可以将其有效去除。
Light chain related impurity 主要产生于轻链的断裂,重链的断裂以及二硫键的断裂过程中 (图2-16)[9]。该案例中,借助 Capto Adhere 的疏水作用与氢键作用,上样量高达 100 g/L resin,在 pH 5.9 ± 0.2,电导小于 7 mS/cm 的条件下,采用流穿的方式进行层析,结果如图2-17 所示, HPSEC Fragment 含量仅为 0.1%, RPLC Fragment 含量仅为 2.5%,符合生产要求,并顺利完成 500 L 以及 2000 L Run。
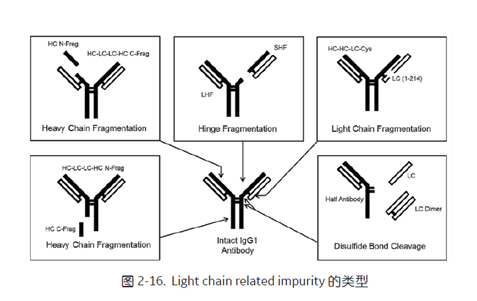
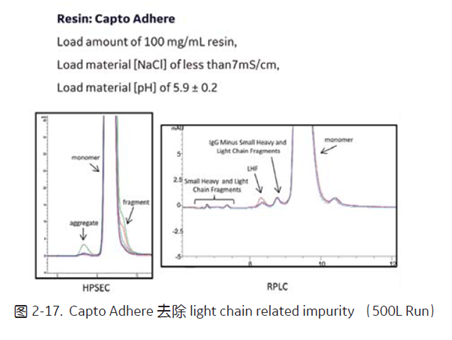
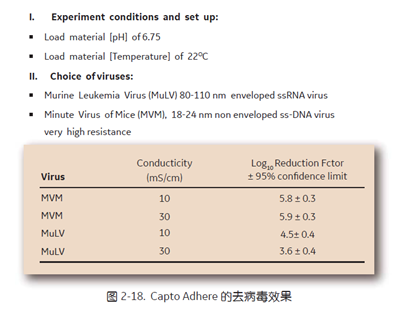
值得注意的是, Capto Adhere 取代了传统的阴离子层析,也同时保留了阴离子流穿模式病毒去除的效果, 图2-18中可以看出,即使上样 pH 高达 6.75,电导在 10~30 mS/cm 的条件下, Capto Adhere 对 MVM 的去除能力接近 6 个 log 降,对 MuLV 的去除能力也在 4 个 log 降左右。可见, Capto Adhere 依然保有强势的去病毒能力。
2.3.2 Capto Butyl ImpRes/Butyl Sepharose High Performance
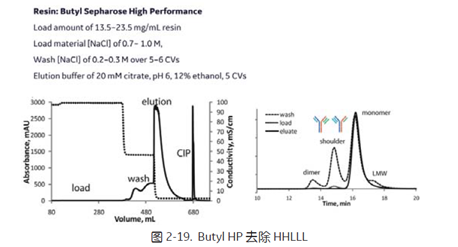
对于极其难以去除的 HHLLL (完整 BsAb 上多了一条轻链),也可以在高分辨率的疏水性较弱的 Butyl Sepharose HighPerformance 上采用结合洗脱的模式进行有效去除 (图2-19)[10]。最终纯度可达 98.2 ± 0.3% ,同时收率在 80% 左右。
Aggregate,在对称型的 IgG-like BsAb 中更容易形成,因为肽链的延伸提高了肽链的长度和灵活性,加剧了分子之间的肽链缠绕。有时候 aggregate 的含量可高达 50%,甚至更高。尽管 aggregate 的结合力比目标 BsAb 只略强一些,仍然可以使用亲和层析去除大部分 aggregate,在洗脱液中添加 PEG/CaCl2 或者 PEG/NaCl 可显著提高目标 BsAb 与 aggregate的分离度。当然,在不添加任何添加剂的情况下,依然通过电荷或/及疏水性差异也可以将其去除殆尽。
2.4.1 Capto MMC ImpRes
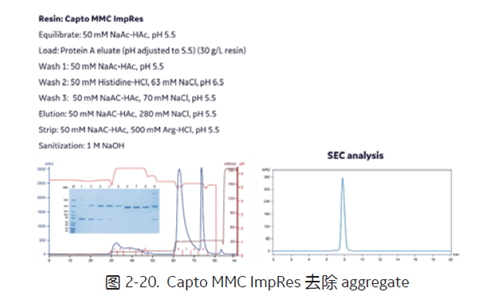
Capto MMC ImpRes 具有更细的粒径和更低的配基密度,从而可以提高单体和聚集体的分辨率。该填料在 pH 5.0-7.0、 0-150 mM NaCl 之间可以保证比较高的结合载量,在 pH 5.0 条件下,获得的纯度最高。通过盐洗脱的方式可以有效去除 aggregate,但是洗脱峰拖尾比较严重,可能是因为疏水作用力在起作用,此时可以用过添加精氨酸 arginine(破坏电荷相互作用和疏水相互作用) 的方式,在保障分辨率的前提下缩小洗脱体积。在图2-20 案例中,采用 50 mM NaAc-HAc, 500 mM Arg-HCl, pH 5.5 的 strip 条件,高效去除了 aggregate,经 HPLC 分析之后, SEC 纯度从 73.3% 提高到了99.0%[7]。
Capto Adhere,是另一种可以有效去除聚集体的复合模式强阴离子填料。它的配基具有 AEX、 HIC 和氢键相互作用等。Capto Adhere 一般以 FT 模式进行聚集体的去除,聚集体的去除效果主要受到 pH,电导和上样量的影响。一般而言,pH 越高,电导越高和/或载量越低更加有利于提高聚集体的去除率。如果 FT 模式无法去除,也可以尝试 B-E 模式。
2.4.2 Capto Phenyl ImpRes
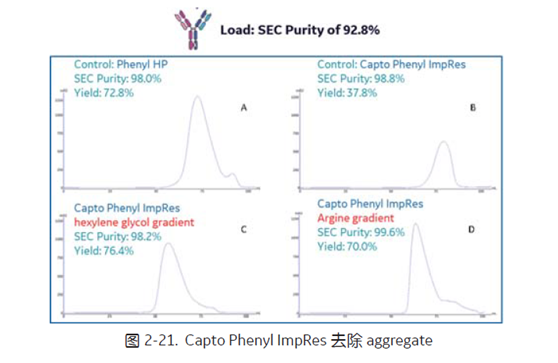
疏水层析技术在 aggregate 去除的应用上非常有效。一般情况下, HIC 可以使 BsAb monomer 通过 FT 模式实现与聚集体的分离。聚集体的疏水性比单体要强,对于自身疏水性比较强的 BsAb 分子, Capto Octyl, Capto Butyl 等疏水性比较弱的可以作为优先选择,通过筛选一个合适的上样条件,就可以使目标 BsAb 分布在流穿组分中, aggregate 结合在填料上,从而实现有效分离。当然,也可以选用 Capto Phenyl ImpRes 或 Phenyl HP 这样高分辨率的疏水层析填料,通过结合洗脱的方式,高效去除 aggregate,纯度都可达 98% 以上,同时可以通过添加乙二醇或精氨酸的方式提高收率 (图2-21)[11]
2.4.3 Capto SP ImpRes/SP HP
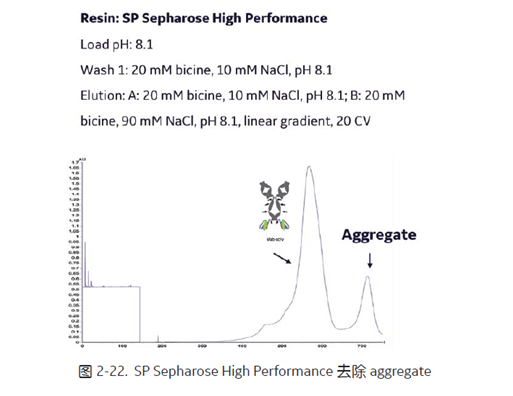
CEX,在碱性 pH 条件下,可以提高对 aggregate 的分辨率 (图2-22)。案例中目标分子为 Mab-ScFv,上样 pH 为8.1,接近目标 BsAb 的 pI,采用结合洗脱的方式,通过在 SP Sepharose High Performance 上进行盐线性梯度洗脱,使得最终SEC 纯度高达 99.3%,收率也近 70%[12],不仅有效去除了 aggregate,同时还除去了杂质 Mab-diabody。
也可以通过在 CEX (Capto SP ImpRes) 的淋洗和洗脱buffer中添加 5%PEG3350 的方式, PEG 的存在下, aggregate 结合的更牢,基本上会在 strip 中洗脱,从而增强在酸性条件下 (pH 5.5) 进行盐梯度洗脱对聚集体的去除效果,显著提高目标 BsAb 与 aggregate 分辨率。
3. Non IgG-like BsAb 的下游纯化策略
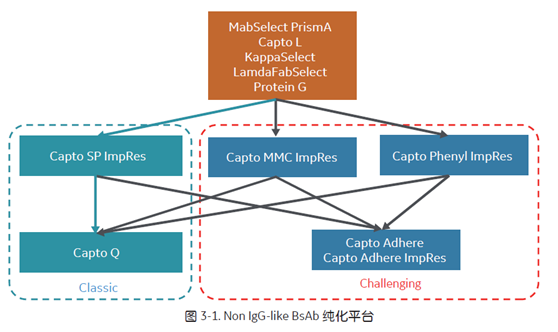
Non IgG-like BsAb,是相对较简单设计的分子,多个抗原结合单元 (即抗体片段) 结合在一个没有 Fc 区域的分子上,从而避免了链交联问题。结构简单且不存在 Fc 段的糖基化问题,故可通过低真核和原核表达系统,表达 1-2 多肽链来生产,从而具有高产和降低成本的优势。我们对此类BsAb给出了相应的纯化路线图,如图3-1,可以去除此类 BsAb中的常见产品相关杂质。
3.1 Non IgG-like BsAb 的亲和捕获
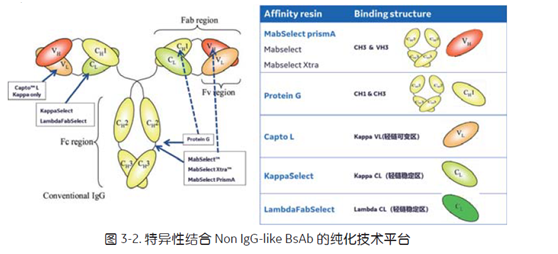
针对 Non IgG-like BsAb,通过亲和捕获一步即可达到较高的纯度和回收率 (图3-2)。
MabSelect PrismA 耐碱改构的蛋白 A 配基,不仅可以结合 Fc 片段,还跟 MabSelect、MabSelect Xtra 一样,可以结合重链可变区 VH,因此能够特异性结合抗体片段 VHH,即可以对纳米抗体进行高效捕获;
来源于链球菌的 Protein G 能高特异性的与 IgG 的 Fc 片段和 CH1 结构域结合,也适用于纯化 Fab 片段;
Capto L 将L蛋白偶联于高流速琼脂糖骨架,L 蛋白能够高特异性的结合 kappa 轻链的可变区,可用于对相应 ScFv、Fab、Dab 等的亲和捕获;
KappaSelect 能高特异性结合 kappa 轻链恒定区,而 LambdaFabSelect 能特异性结合 Lambda 轻链恒定区,一步可以达到高纯度和高回收率。
3.1.1 MabSelect PrismA 捕获 VHH 及 Fab
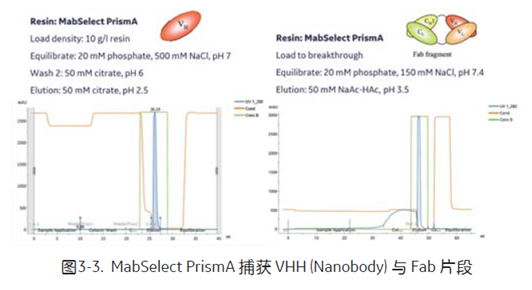
MabSelect PrismA 与 VHH 片段高特异性结合,能够对纳米抗体进行高效捕获 (图3-3),那么对于含有 VH 片段的Fab片段而言, MabSelect PrismA 同样具备特异性结合的能力,都能够高效捕获,达到较高的纯度和回收率。
3.2 Non IgG-like BsAb 的精纯
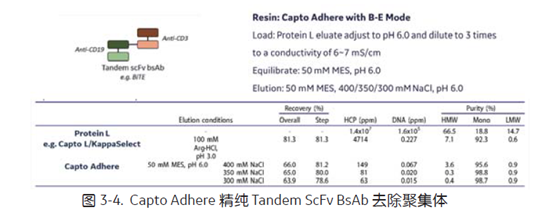
3.2.1 Capto Adhere 精纯 Tandem ScFv BsAb
对于抗体药而言,仅一步亲和是远不够的,多模式复合填料 Capto Adhere 能一步去除内毒素, DNA,聚集体, HCP等。图3-4 中,在继 Protein L (Capto L/KappaSelect) 对 Tandem ScFv BsAb 特异性捕获之后,采用 Capto Adhere 的结合洗脱模式,优化洗脱条件,改变洗脱盐浓度,平衡纯度与回收率。最终在保障回收率的前提下,去除了大量的残留聚集体,将 Tandem ScFv BsAb 的单体纯度从 92.3% 提高到 98.8%,满足工业生产需求[13]。
3.3 Case Study – Total Process
Non IgG-like BsAb 纯化的成功案例有很多,不乏成功应用 MabSelect PrismA, Capto L, KappaSelect, LambdaFab Select 等进行捕获的工业级别案例,同时精纯步骤,高分辨率的阳离子与多模式复合填料也都得到了广泛应用。
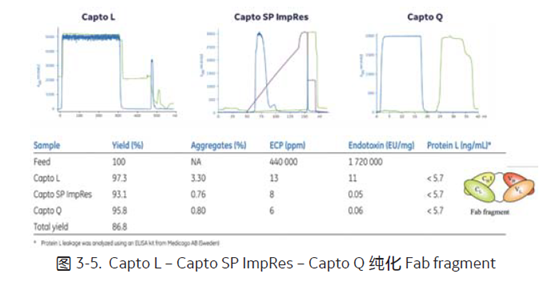
图3-5 中, Capto L 高效捕获含有 kappa 轻链的可变区的 Fab 片段,一步亲和收率高达 97.3%,经阳离子层析Capto SP ImpRes 和阴离子层析 Capto Q 之后, Fab 纯度高达 99.2%,同时 total 收率高达 86.8%。
同样, Capto L 能够高效捕获仅含有 kappa 轻链的可变区的 Dab 片段 (图3-6),一步亲和收率高达 99.6%,经高分辨率多模式层析填料 Capto MMC ImpRes (B-E) 和高分辨率多模式层析填料 Capto Adhere ImpRes (FT) 之后,有效去除大肠表达 Dab 过程中伴随的 ECP 和内毒素等杂质,获得高纯 Dab,同时三步层析总收率高达 80.8%。
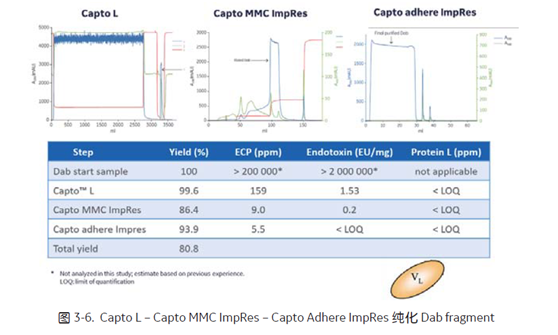
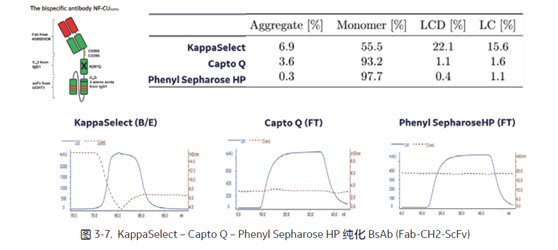
图3-7 中,对于自行构建的特殊 Non IgG-like BsAb (Fab-CH2-ScFv)[14], KappaSelect 高特异性结合其 kappa 轻链恒定区,高效捕获该 BsA b分子,后续通过 Capto Q 和 Phenyl Sepharose HP 的流穿模式,简单高效的去除了大量的 LCD, LC以及 aggregate 杂质。最终 Fab-CH2-ScFv 的 SEC 纯度高达 97.7%,满足工业生产需求。
因 Non IgG-like BsAb 结构相对简单,没有 Fc 区域的糖基化修饰等蛋白翻译后加工,因此可以选用大肠杆菌和酵母等表达体系,目前上市的抗体类似药物也不乏使用此类表达体系的产品,如:罗氏的 Ranibizumab、 UCB 的 certolizumab pegol、阿斯利康的 moxetumomab pasudotox-tdf、诺华的 brolucizumab 以及赛诺菲的 Caplacizumab-Yhdp;2020年 FDA 也批准了丹麦灵北制药预防偏头疼药物 Eptinezumab,迎来了首个以酵母为表达载体的单抗药物。使用酵母或者大肠的表达平台显然其生产的成本是要优于哺乳动物细胞平台,培养周期短,可以进行高密度的大规模发酵,而且也省去了后期病毒清除验证的成本,大大的减少了研发周期,在成本控制战激烈的当下也不失为一个新的研究方向。
从分子设计的角度,研究者为了实现更方便的纯化策略也经常会添加 Tag,而经常使用的就是 6*His,使用了这种Tag 的双抗分子可以使用 IMAC Sepharos 6 Fast Flow 或者 Ni Sepharose 6 Fast Flow 亲和类填料进行专一高效捕获,实现平台化的纯化策略。另外因 Non IgG-like BsAb 分子较小,容易实现组织浸润,穿透血脑屏障而实现疾病治疗,往往其半衰期较短,为了延长半衰期研究者们通常进行 Fc 或者 HSA 融合的方式构建分子,如果使用了 Fc 融合的方式其下游纯化可以参考 IgG-like 的分子的纯化方式;HSA 融合分子则可以使用 Capto Blue 亲和层析填料搭建纯化平台;另外也有几款上市的 PEG 融合抗体片段分子来延长其半衰期,针对 PEG 融合蛋白, 高分辨率离子填料 Capto SP ImpRes 或者Capto Q ImpRes 则可用来进行游离 PEG 的去除精纯。
当然,使用了不同的上游表达平台,下游纯化目标的设定也会做出相应调整以满足不同的产品相关杂质去除要求,比如使用了大肠杆菌的平台则下游纯化对于内毒素去除能力的挑战就会相应的变高,因此在纯化平台的考量上则侧重于选择特异性更强的复合模式填料如 Capto MMC ImpRes 和 Capto Adhere ImpRes,同时对于色素的去除能力也有更优的表现[16],也正是由于其在色素、内毒素去除及分辨率上更优的表现,高分辨率复合模式层析填料成为了越来越多的纯化具有挑战性蛋白的平台填料。
BsAb 的纯化中,最大的挑战不仅存在于杂质的去除步骤,还存在于批次稳定性上,特别是双抗工艺大量使用复合模式填料和疏水填料,多为结合模式,批次的差异性尤其需要引起我们的关注,在早期搭建稳定的工艺,才能顺利放大工艺。
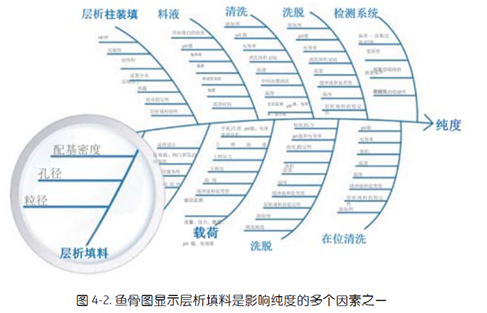
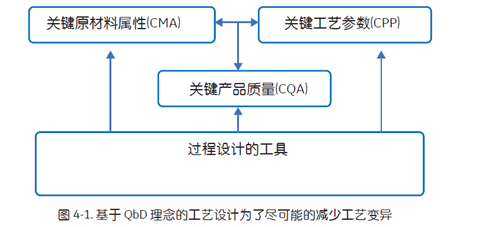
在 PC 阶段工艺表征的时候,通常填料的批次差异也会被考虑进去 (图4-1),但是在以前使用 DoE 进行工艺确认的时候,没有合适的 kit 无法将填料的变异进行有效量化。
在鱼骨图中 (图4-2),尽管已经分析出填料的批次差异对于工艺的影响是较为显著的,但是无法真正进入 DoE 的实验,客户常用的方式就是随机选择三批次的填料进行稳健性测试,但是这种做法局限性是非常明显的。局限性表现在三个方面:a 如果没有观察到不同批次的变异,不代表没有影响,可能选择的批次配基密度太类似,而时间关系很难能拿到靠近极端范围的填料批次。b 如果观察到变异,但是无法量化,趋势未知,从而不能指导工艺范围的调整及优化。c 对于变异的引起是来源于填料批次还是其他问题,并不能清楚,很可能有噪音干扰,从而导致这种测试仅仅起到有限的参考作用。
1. Labrijn A.F, et al., Bispecifc antibodies: a mechanistic review of the pipeline. Nature Review Drug Discovery, 2019.
2. Schaefer, W., et al., Immunoglobulin domain crossover as a generic approach for the production of bispecifc IgG antibodies.Proc Natl Acad Sci U S A, 2011. 108(27): p. 11187-92.
3. Bengt W., et al., Development of a single-step, protein A chromatography process for bispecifc antibodies in early screening.Summit.
4. Yifeng L., A brief introduction of IgG-like bispecifc antibody purifcation: Methods for removing product-related impurities.
Protein Expression and Purifcation, 155 (2019) 112-119.
5. Skegro D., et al., Immunoglobulin domain interface exchange as a platform technology for the generation of Fc heterodimers and bispecifc antibodies. J Biol Chem, 2017. 292(23): 9745-9759.
6. Sharkey B., et al., Purifcation of common light chain IgG-like bispecifc antibodies using highly linear pH gradients, mAbs9 (2017) 257–268.
7. Jiaqin T., et al., Removal of half antibody, hole-hole homodimer and aggregates during bispecifc antibody purifcation using MMC ImpRes mixed-mode chromatography. Protein Expression and Purifcation 167 (2020) 105529.
8.Purifcation-of-bi-specifc-monoclonal-antibodies-mAbs-A-case-study_KA4159040518PP.
9. Ellen O’C., et al., Monoclonal antibody fragment removal mediated by mixed mode resins. Journal of Chromatography A, 1499 (2017) 65–77.
10. Rachel B W., et al., Analytical characterization of a monoclonal antibody therapeutic reveals a three-light chain species that is efcientlyremoved using hydrophobic interaction chromatography, mAbs 5 (2013) 925–935.
11. Troii H., et al., Use of mobile phase additives for the elution of bispecifc and monoclonal antibodies from phenyl based hydrophobic interaction chromatography resins, Journal of Chromatography B 1096 (2018) 20–30.
12. Troii H., et al., Alkaline cation-exchange chromatography for the reduction ofaggregate and a mis-formed disulfde variant in a bispecifc antibodypurifcation process, Journal of Chromatography B, 975 (2015) 1–8.
13. Serene W., et al., Investigation of the effect of salt additives in Protein L afnity chromatography for the putifcation of tandem single-chain variable fragment bispecifc antibodies, mAbs, 12 (2020) 1-10.
14. Neumann G., Downstream Process Development and Preliminary Formulation Development for the Bispecifc Antibody NF-CU N297Q for a Clinical Phase I/Iia Trial, Ph.D. thesis University of Tübingen, 2016.
16. A platform approach for the purifcation of domain antibodies (Dabs) 29065541AB
17. 白皮书:生物治疗药物纯化过程中的质量源于设计:理解并解决工艺变异性的来源